Mikrobiom jelit to termin używany do opisania drobnoustrojów żyjących w przewodzie żołądkowo-jelitowym. Mikroby te są bardzo różnorodne i obejmują wirusy, bakterie, pierwotniaki, grzyby i archeony. Donoszono, że drobnoustroje w jelitach są równe liczbie komórek samego gospodarza (Sender, Fuchs i wsp. 2016). Co ważne, mikrobiomy jelitowe odgrywają co najmniej 3 krytyczne role w gospodarzu, w tym zapewniają ochronną barierę jelitową, trawienie i metabolizowanie składników odżywczych oraz regulację odporności (Wykres 1). Wiele zmiennych wpływa na kolonizację jelita świń przez kilka pierwszych tygodni życia, w tym mikrobiom pochwy, skóry i kału lochy, mleka i paszy, warunki w kojcu i na porodówce, infekcje wirusowe i bakteryjne, iniekcje leków przeciwbakteryjnych i stres podczas zabiegów na prosiętach lub podczas transportu. Te zdarzenia mogą odgrywać rolę w kształtowaniu mikrobiomu przez cały okres życia świni produkcyjnej (Niederwerder 2017). Związek i równowaga między drobnoustrojami jelitowymi jest złożony i słabo poznany w stanach zdrowia lub chorobach. Jednak coraz więcej dowodów potwierdza rolę drobnoustrojów jelitowych jako głównych graczy w przypadkach choroby.
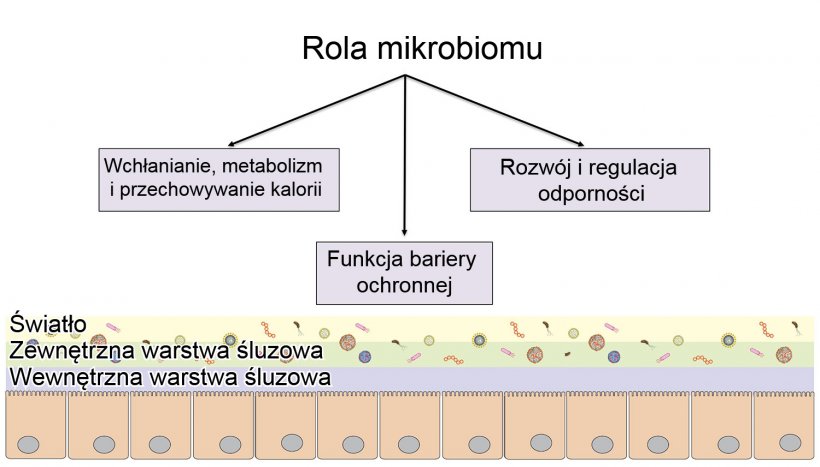
Rola mikrobiomu: zapewnienie ochronnej bariery jelitowej, trawienie i metabolizowanie składników odżywczych oraz regulacja odporności.

Transplantacja mikroflory kałowej lub FMT to proces pobierania kału od zdrowego dawcy i przeszczepiania go chorym osobnikom. Podobnie jak w przypadku transplantacji narządów, celem FMT jest poprawa zdrowia biorcy przeszczepu. W procesie FMT nie tylko przeszczepia się żywe i martwe drobnoustroje, ale także małe cząstki paszowe, komórki z jelita cienkiego i grubego oraz produkty metaboliczne bakterii (Bojanova i Bordenstein 2016). Mechanizm, według którego FMT jest skuteczny, jest słabo zdefiniowany dla większości chorób. Uważa się jednak, że korzyści płynące z FMT wynikają ze zwiększenia liczby korzystnych mikroorganizmów, zwiększenia różnorodności drobnoustrojów i stymulacji odporności śluzówkowej (Niederwerder 2018)
U ludzi FMT jest najczęściej stosowany jako narzędzie terapeutyczne w nawracających zakażeniach Clostridium difficile, które nie reagują na leczenie przeciwdrobnoustrojowe (Gough, Shaikh i wsp. 2011). Jednakże FMT został ostatnio uznany za potencjalną terapię dla szerokiej gamy innych chorób u ludzi, takich jak zespół jelita drażliwego, oporność na środki przeciwdrobnoustrojowe patogenów w przewodzie pokarmowym, zespół metaboliczny i insulinooporność (Bakker i Nieuwdorp 2017). U zwierząt FMT lub transfaunacja została również wykorzystana jako narzędzie terapeutyczne dla szeregu chorób, takich jak infekcja parwowirusem u psów, powikłaniach pooperacyjnych przemieszczenia trawieńca u bydła i zapalenie jelita grubego u koni (Niederwerder 2018). Oprócz terapeutycznego potencjału FMT u zwierząt, badano także profilaktyczne i immunogenne zastosowania FMT. Przykładowo, FMT zostało zbadane jako potencjalne narzędzie do zwiększenia wydajności wykorzystania paszy zarówno u drobiu, jak i trzody chlewnej (Niederwerder 2018).
Praca w moim laboratorium skupiała się na badaniu wykorzystania mikrobiomu jelitowego i FMT w zapobieganiu i kontroli choroby związanej z cirkowirusem świń (PCVAD). PCVAD jest eksperymentalnie odtwarzany za pomocą modelu koinfekcji wirusa zespołu rozrodczo- oddechowego świń (PRRSV) i cirkowirusa świń typu 2 (PCV2). Współzakażenia PRRSV i PCV2 są powszechne i powodują znaczne straty ekonomiczne w produkcji wieprzowiny na całym świecie. Mikrobiom jelitowy stanowi alternatywne narzędzie do kontroli i zapobiegania chorobom powodowanym przez te koinfekcje. Nasza początkowa praca wykazała, że zwiększona różnorodność mikrobiomów jelitowych wiązała się z poprawą wyników klinicznych świń współzakażonych PRRSV i PCV2 (Niederwerder, Jaing i wsp. 2016, Ober, Thissen i wsp. 2017). Lepsze wyniki charakteryzowały się świniami mającymi mniej objawów klinicznych i zwiększonym przyrostem masy ciała.
Ze względu na konsekwentne korzyści różnorodności drobnoustrojów we współzakażeniu odkryte w naszej wczesnej pracy, niedawno zbadaliśmy FMT jako narzędzie zapobiegawcze dla PCVAD (Niederwerder, Constance i wsp. 2018). Kał pobierano od 2 loch - dawczyń, charakteryzującymi się wysokim zdrowiem i wydajnością, w tym licznymi miotami, dużą liczbą urodzonych żywo prosiąt, niską śmiertelnością przed odsadzeniem, brakiem mumifikatów w miotach i nie wykonywanej ostatnio terapii przeciwdrobnoustrojowej. Dziesięć par miotów było podzielonych na grupy FMT i kontrolną. Materiał przeszczepowy dostarczano prosiętom z grupy FMT przez 7 kolejnych dni przed jednoczesnym zakażeniem PRRSV i PCV2. Zakażone świnie porównano ze świniami kontrolnymi. Nasze wyniki wykazały, że świnie, które otrzymały FMT, mały mniejsze objawy kliniczne związane z PCVAD, zmniejszoną replikację wirusa PRRSV i PCV2, lepszee przyrostem masy ciała i zwiększoną produkcję przeciwciał przeciw obydwu wirusom (Niederwerder, Constance i wsp. 2018).
Ogólnie rzecz biorąc, mikroorganizmy jelitowe i przeszczep mikroflory kałowej są obiecującymi narzędziami, które można wykorzystać do poprawy zdrowia świni i zapobiegania chorobom, takim jak te związane z zakażeniem PCV2.





