Rekombinacja jest zjawiskiem naturalnym i motorem ewolucji genetycznej PRRSV. Występowanie rekombinacji odnotowano w eksperymentach laboratoryjnych na hodowlach komórkowych od końca lat 90-tych. Aby doszło do rekombinacji, dwa wirusy muszą zainfekować komórkę i replikować się, wymieniając między sobą materiał genetyczny i uzyskując nowego wirusa potomnego (rysunek 1).
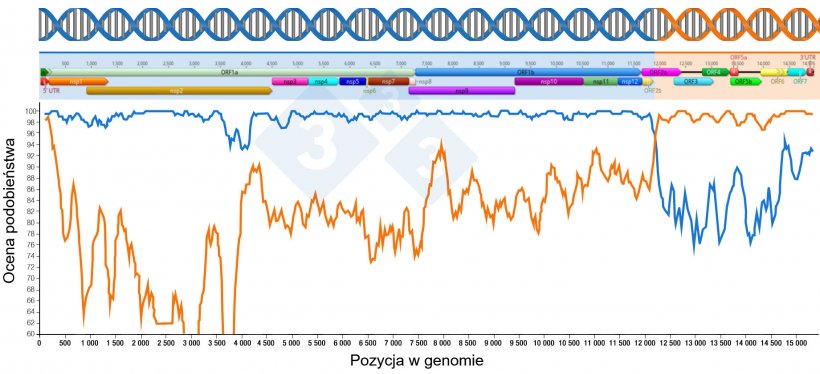

W najnowszej literaturze donoszono, że rekombinacja miała miejsce między:
- Wirusami typu dzikiego
- Wirusami z atenuowanej szczepionki - Modified Live Vaccine (MLV)
- Wirusami typu dzikiego i szczepionkowymi
Zdarzenia rekombinacji mogły zawsze występować w terenie, ale to, co zmieniło się w ostatnich latach, to nasza zdolność do wykrywania takich zdarzeń poprzez zwiększone wykorzystanie sekwencjonowania nowej generacji, NGS (jak wyjaśniono w artykule opublikowanym na 3trzy3.pl „Diagnostyka molekularna PRRS: kiedy sekwencjonowanie tylko 4% nie wystarcza”) oraz dostępność narzędzi bioinformatycznych do analizy rekombinacji.
Wiele zdarzeń rekombinacji, które występują w terenie, może generować niezdolne do przetrwania wirusy lub wirusy, które nie są w stanie ustanowić stabilnej infekcji i przetrwać w populacji. Większe zagrożenie dla zdrowia zwierząt wynika z rekombinacji dwóch różnych wirusów typu dzikiego (rysunek 2).
Nowo pojawiające się szczepy Rosalia i L1C.5 są przykładami agresywnych wirusów PRRS typu dzikiego, które endemicznie zadomowiły się w populacji świń i spowodowały poważne objawy kliniczne.
W tej sytuacji pozostajemy z pytaniami:
- Dlaczego istnieje przekonanie o większej liczbie rekombinowanych wirusów PRRSV pochodzących ze szczepionek atenuowanych (MLV)?
- Co się stanie z nowym wirusem?
Zalecenia w ulotkach MLV dotyczą stosowania u zdrowych zwierząt w celu rozwinięcia indywidualnej odporności przed zakażeniem wirusem typu dzikiego. W walce z wirusem PRRSV typu dzikiego, wirusy atenuowane często krążą razem z wirusami typu dzikiego. Pochodzące z atenuowanego wirusa rekombinowane wirusy nie są tak agresywne jak wirusy typu dzikiego lub rekombinanty typu dzikiego (rysunek 2).
W Stanach Zjednoczonych doniesienia o przypadkach opisujących zastosowanie środków, takich jak wzmocnienie biokontroli i praktyk bezpieczeństwa biologicznego w celu uniknięcia rozprzestrzeniania się wirusa w pomieszczeniach porodowych i poprawy indywidualnej odporności prosiąt, wykazały obiecujące wyniki w zmniejszaniu klinicznych skutków tych nowo pojawiających się wirusów PRRSV-2 pochodzący ze szczepionki. W Europie doniesiono również, że rekombinowany atenuowany szczepionkowy wirus PRRSV-1 nie jest tak łagodny jak atenuowany wirus, ani tak agresywny jak wirus typu dzikiego w eksperymentach klinicznych.
Rekombinowane wirusy chimeryczne PRRSV-2 wytwarzane w laboratorium między wirusami typu dzikiego i szczepionkowymi atenuowanymi oraz podawane doświadczalnie u świń w warunkach eksperymentalnych miały mniej wyraźne objawy kliniczne w porównaniu z wirusami typu dzikiego, ale objawy kliniczne nie były tak łagodne jak te powodowane przez niezmienionego wirusa szczepionkowego (rysunek 2). Ponadto istnieją również doniesienia, w których pozyskane w terenie wirusy rekombinowane typu dzikiego między szczepionkami atenuowanymi a szczepami terenowymi były problematyczne w hodowli komórkowej.
Ryc. 2: Konsekwencje kliniczne i zdolność bioinformatyczna do wykrywania zdarzeń rekombinacji między różnymi wirusami PRRSV.
| Szczep PRRS | Konsekwencje kliniczne |
Zdolność bioinformatyczna do wykrywania rekombinacji |
|---|---|---|
| Wirus atenuowany (MLV) |  |
 |
| Rekombinant MLV & MLV | ||
| Rekombinant MLV i dziki-PRRSV | ||
| Typ dziki PRRSV (wt-PRRSV) | ||
| Rekombinant wt-PRRS i wt-PRRSV |
Innym podejściem stosowanym w niektórych krajach do zarządzania PRRSV jest wprowadzenie inokulum żywego wirusa (LVI), które obejmuje pobieranie próbek (takich jak surowica lub płuca) bezpośrednio z terenu, potwierdzenie obecności PRRSV za pomocą RT-PCR, rozcieńczenie próbek w pożywce i wystawienie zwierząt na działanie wirusa terenowego obecnego w gospodarstwie.
Wirusy dzikie nie są atenuowane, tak jak MLV, co więcej LVI może nieświadomie zawierać wiele szczepów PRRSV, tworząc okazję do rekombinacji wirusów typu dzikiego
Ponadto, użycie próbek LVI nie jest prawnie zatwierdzone w wielu krajach i może zawierać inne patogeny krążące w krwiobiegu dawców, np. cirkowirusy świń, parwowirusy świń itp.
Jakie są konsekwencje występowania wielu szczepów PRRS i/lub rekombinantów?
-
Stada hodowlane zakażone ≥ 3 szczepami PRRSV miały o 1837 więcej strat prosiąt na 1000 loch w porównaniu ze stadami zakażonymi ≤ 2 szczepami, co potwierdza fakt, że im więcej szczepów PRRSV krąży w populacji/stadzie/świniach, tym większy jest wpływ/objawy kliniczne (im więcej = tym gorzej);
-
Stada hodowlane, w których wykryto ≥ 3 szczepy PRRSV podczas eliminacji PRRSV, potrzebowały 12 tygodni więcej, aby osiągnąć stabilność w porównaniu ze stadami, w których wykryto ≤ 2 szczepy;
-
Stada, w których zidentyfikowano rekombinowanego wirusa PRRSV w czasie wybuchu choroby, miały o 1,827 wyższe straty prosiąt na 1000 loch w porównaniu z gospodarstwami, w których nie wykryto przypadków rekombinacji.
Kontrolowanie PRRS może pomóc ograniczyć występowanie zdarzeń rekombinacji
Niektóre przykłady to:
-
Unikanie wprowadzania loszek, które są zakażone innym wirusem PRRSV niż ten, który jest obecnie obecny w stadzie hodowlanym;
-
Unikanie mieszania świń hodowlanych i tuczników zakażonych różnymi wirusami PRRSV typu dzikiego
-
Badanie próbki LVI za pomocą NGS przed podaniem i unikanie używania materiału LVI zawierającego wiele genetycznie różnych wirusów PRRSV
-
Jeśli materiał LVI zawiera wirusa podobnego do MLV, użyj wirusa MLV zamiast wirusa terenowego.
-
Podczas stosowania atenuowanego wirusa należy unikać mieszania lub wstrzykiwania dwóch atenuowanych wirusów jednocześnie. Należy również unikać rotacji szczepionek atenuowanych w obrębie stada lub przepływu produkcyjnego
-
Należy przestrzegać zaleceń szczepionkowych MLV dotyczących stosowania u zdrowych zwierząt w celu wywołania indywidualnej odporności przed spodziewanym zakażeniem wirusem typu dzikiego.
Wirus PRRSV jest bardzo poważnym czynnikiem zagrażającym zdrowiu zwierząt i z upływem czasu ewoluuje genetycznie. Kontrolowanie PRRSV nie tylko prowadzi do lepszych wyników w zakresie produktywności, ale także zmniejsza możliwości rekombinacji różnych wirusów typu dzikiego i tworzenia bardziej agresywnych.




