Streptokokoza świń jest endemicznym problemem chorobowym wywoływanym przez Streptococcus suis (S. suis), rozpoznawanym głównie przez neurologiczne objawy kliniczne związane z zapaleniem opon mózgowych, sztywnością stawów i śmiertelnością w fazie poodsadzeniowej (Lun i wsp., 2007; Goyette-Desjardins i in., 2014). Wystąpienie objawów chorobowych jest poprzedzone kolonizacją migdałków i dróg oddechowych (Gottschalk i Segura, 2019), są także doniesienia o zakażeniach drogą pokarmową (Swildens, 2009). Na temat tej ostatniej drogi zakażenia ciągle się dyskutuje, jednak niskie pH żołądka stanowi silną barierę dla modeli zakażeń pokarmowych (Warneboldt i wsp., 2016).
Mimo tego, że wiele wiadomo na temat choroby, wciąż brakuje powtarzalnego modelu, który naśladuje naturalną infekcję. Cytując Segurę i in. (2016), „początkowe etapy patogenezy infekcji S. suis były zaniedbanym obszarem badań”. Co więcej, S. suis utrzymuje się w systemach produkcji trzody chlewnej od wielu lat i wciąż brakuje szczepionek. Jedynym stosowanym typem są bakteryny autogenne, ale wyniki ich skuteczności często są sprzeczne. Szczepienie prosiąt pochodzących od immunizowanych macior prawdopodobnie nie zapewnia ochrony ze względu na interferencje z przeciwciałami matczynymi (Baums et al., 2010). Bierna matczyna odporność może chronić potomstwo (Rieckmann i wsp., 2020), ale badania wskazują, że eliminacja matczynych przeciwciał S. suis następuje przed odsadzeniem, niezależnie od tego czy locha była zaszczepiona czy przechorowała (Corsault i wsp., 2021).

Jeśli zapytamy hodowców o występowanie S. suis, słyszymy: „Mamy niewiele przypadków w każdym rzucie, ale czasami mamy epidemie”. Ponadto rośnie obawa, że ograniczenia w stosowaniu środków przeciwdrobnoustrojowych mogą pogorszyć sytuację. Podjęto wysiłek zebrania doświadczeń terenowych lekarzy weterynarii i opublikowanych dotychczas badań dotyczących ryzyka wystąpienia choroby, które wygenerowały listę pytań. Zaproponowano hipotezę podobną do równania opisującą podsumowanie potencjalnych czynników przyczyniających się do zmniejszonego lub zwiększonego ryzyka wystąpienia choroby (ryc. 1).
Rycina 1. Hipoteza podobna do równania opisująca niektóre potencjalne czynniki przyczyniające się do zmniejszonego lub zwiększonego ryzyka choroby paciorkowcowej u prosiąt.
|
Możliwość zachorowania= [(PRZYPADKI0.1-10%/NOSICIELE0-100%)1× Nieznany wyzwalacz zjadliwości] + WSPÓŁINFEKCJE%?2+POZBAWIONE SIARY%?3 + STRES (transport & mieszanie miotów)0-30%4 +SŁABA WENTYLACJA%? + TEMPERATURA%? + INNE? - ANTYBIOTYKI90%? - SZCZEPIONKI AUTOGENICZNE0-30%?5 - WCZEŚNIEJSZY KONTAKT S. suis%?6 - DODATKI ŻYWIENIOWE%?7 - INNE? |
1Powszechnie wiadomo, że przypadki i wielkość epidemii znacznie się różnią, podczas gdy częstość występowania wirulentnych szczepów S. suis może być nadal wysoka.
2Grypa świń zwiększa podatność (Meng i wsp. 2015; Meng i wsp., 2019), a PRRSv, świński cirkowirus oddechowy, Bordetella bronchiseptica, S. suis lub Haemophilus parasuis mogą zwiększać częstość występowania choroby, odsetek płuc ze zmianami chorobowymi, nasilenie zmian i wolniejsza rekonwalescencja niż w przypadku samej infekcji jednym patogenem (Segura i wsp., 2020).
3W modelach eksperymentalnych S. suis często wykorzystuje się świnie urodzone przez cesarskie cięcie, pozbawione siary (Ferrando i in., 2014; Dekker i in., 2017). Chociaż poziom lub próg spożycia siary potrzebny do wpłynięcia na podatność jest nadal nieznany.
4Niektóre modele obejmujące czynniki stresorowe zwiększyły odsetek udanych modeli infekcji (Swildens i in., 2004; Swildens, 2009; Ferrando i in., 2015).
5Hopkins i in. (2019) przebadali 24 kohortowe badania terenowe metodą regresji Coxa i regresji logistycznej, w których ogólna skuteczność szczepionki autogennej wynosiła odpowiednio 27% i 21%. Corsaut i wsp. (2021) doszli do wniosku, że autogeniczny program szczepień loch i loszek może zwiększać przeciwciała, ale odporność matczyna nie trwała wystarczająco, aby chronić prosięta po odsadzeniu. Dostępne są tylko trzy doświadczenia terenowe wykazujące skuteczność autogennych bakteryn wytwarzanych przez licencjonowane firmy (Torremorell i wsp., 1997; Hopkins i wsp., 2019; Corsaut i wsp., 2020).
6Korzystne może być narażenie na S. suis. Wcześniejsza prowokacja małą dawką S. suis stosowaną do szczepienia świń, ale nie wcześniejsze szczepienie PRRSV, skutkowała niższą częstością występowania choroby paciorkowcowej w modelu koinfekcji PRRSv i S. suis (Schmitt i wsp., 2001). Infekcja o różnych serotypach S. suis lub równoczesna koinfekcja (serotyp 2 i 9) może wpływać na śmiertelność i obciążenie bakteryjne; Obciążenie serotypem 2 i śmiertelność były niższe u świń narażonych na oba serotypy (Dekker i wsp., 2017).
7Correa-Fiz i in. (2020) stwierdzili, że średniołańcuchowe kwasy tłuszczowe w połączeniu z naturalnym środkiem przeciwzapalnym, wykazały równoważne wyniki jak amoksycylina, zmniejszając częstość występowania objawów klinicznych zgodnych z S. suis.
Bez modelu naśladującego naturalną infekcję wydaje się oczywiste, że nadal brakuje nam lepszego zrozumienia podatności gospodarza i czynników wyzwalających zjadliwość S. suis. Autorzy z wyżej wspomnianych niedawnych badań S. suis wskazują, że kluczowe są pierwsze etapy kolonizacji bakterii. Etapy te obejmują rywalizację patogenu z mikrobiotą, opieranie się odporności miejscowej, a wreszcie przyleganie i przekraczanie bariery nabłonkowej błony śluzowej. Potencjalna rola zdrowia i odporności błony śluzowej, w tym interakcje między błoną śluzową, biofilmem i S. suis, otwierają pole do spekulacji na temat dodatków paszowych i interwencji żywieniowych. Jednak wciąż brakuje nam solidnych dowodów.
S. suis jest obecny w dużej liczbie w początkowych odcinkach przewodu pokarmowego, a przenoszenie patogenu następuje w kolejnych fazach produkcyjnych. Murase i in. (2019) wykazali, że mikrobiota śliny obejmuje Streptococcus spp. przy 16,9% (50,1% S. suis) u prosiąt ssących, 18,2% (51,8% S. suis) u świń po odsadzeniu i 9,9% (62,6% S. suis) u macior. Ostatnio zbadano 15 prosiąt z 3 różnych miotów i obserwowaliśmy obciążenia migdałków S. suis serotyp 9 w czasie (ryc. 2). Co ciekawe, 60% prosiąt było poniżej granicy wykrywalności qPCR przed odsadzeniem, ale wszystkie stały się nosicielami w 6 dniu po odsadzeniu. Transmisja i/lub obciążenie S. suis wzrosło po odsadzeniu, podczas gdy 2 naturalnie zakażone świnie, od tej samej lochy, ale z innego kojca, były już nosicielami przed odsadzeniem. Takie wyniki zgadzają się z naszymi wcześniejszymi ustaleniami (Segura i in., 2020). Rycina 2. S. suis s9 w jamie ustnej przed i po odsadzeniu. Liczba S. suis serotypu 9 (średnia wymaz z migdałków i śliny) zmienia się po odsadzeniu dla 15 prosiąt z 3 różnych miotów (przydzielonych jako różne pochodzenie lochy 3/kojec przy odsadzeniu).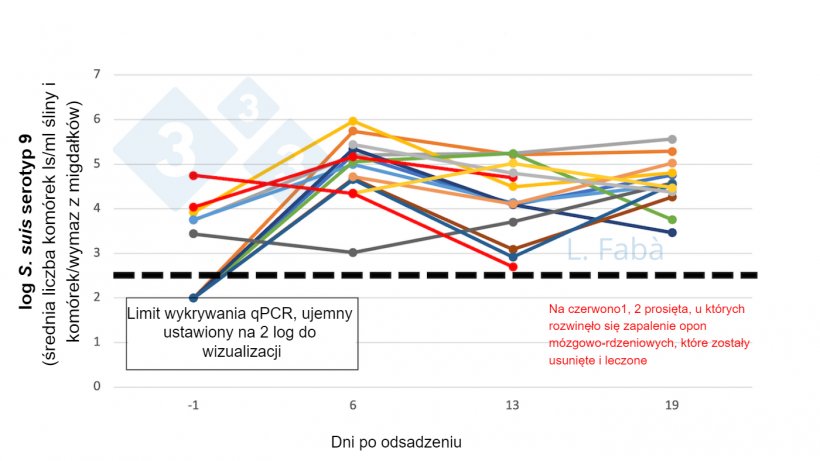
Do tej pory nie wiadomo, czy zmniejszenie liczby nosicieli (transmisji), obciążenia migdałków i kolonizacji przewodu pokarmowego od fazy ssania do fazy odchowu może zmniejszyć ryzyko choroby. Jama ustna i błona śluzowa człowieka stanowią integralną część ogólnego stanu zdrowia, w tym ryzyka chorób posocznicy i dobrego samopoczucia (Lockhart i wsp., 2009; Zawadzki i wsp., 2016). Niektóre ekstrakty roślinne i kwasy tłuszczowe wykazują aktywność przeciw paciorkowcom in vitro (Aguiar et al., 2018; Kovanda et al., 2019). W rzeczywistości higiena jamy ustnej u ludzi zmniejsza ryzyko paciorkowcowe (Okuda i wsp. 1998, Paju i Scannapieco, 2008; Müller, 2015). Takie dowody są trudne do wykazania u świń, ponieważ naturalny model infekcji jeszcze nie istnieje i musi być oceniany w warunkach terenowych i na dużą skalę.
Wells i in. (2019) niedawno zbadali różnice między mikrobiomem migdałków prosiąt w zdrowych miotach a miotami z przypadkami S. suis. Ponadto Ferrando i wsp. (2015) wykazali, że niski poziom glukozy, ale wysoki poziom glukanów w błonie śluzowej może wywołać namnażanie S. suis, co jest ważne, ponieważ glukoza jest szybko wchłaniana, ale glukany z diety utrzymują się w jamie ustno-gardłowej. Patrząc na obraz dyskusji (ryc. 1), czynniki żywieniowe mogą stać się kolejnym ważnym aspektem, a dalsze badania w tym kierunku są uzasadnione.
Choroba pojawia się u zdrowych i dużych prosiąt, które spożywają duże ilości mleka loch i słabo przystosowują się do stałych pasz przed odsadzeniem. Wcześnie, zaraz po odsadzeniu cierpią na niedostateczne wchłanianie składników odżywczych z pewną atrofią kosmków, a następnie (3-7 dni później) nagle spożywają duże ilości paszy. Przyczynia się to do uszkodzenia tkanki jelitowej, w tym stanów zapalnych, zmniejszonego dostarczania tlenu, zwiększonej przepuszczalności nabłonka i zmian w mikrobiocie. Niektóre badania wskazują, że strategie żywieniowe, takie jak wysoka zawartość lucerny, obniżyły liczbę S. suis (Zhang i wsp., 2016) i inne źródło Cu (hydroksychlorek w porównaniu z Cu w postaci siarczanu 160 mg/kg) obniżyły liczbę Streptococcus spp w jelicie grubym (Villagómez -Estrada i in., 2020). Ostatnio Correa-Fiz i in. (2020) stwierdzili, że średniołańcuchowe kwasy tłuszczowe w połączeniu z naturalnym produktem przeciwzapalnym wykazały równoważne wyniki do amoksycyliny w zmniejszaniu częstości występowania objawów klinicznych zgodnych z chorobą powodowaną przez S. suis w porównaniu z peptydem lizozymowym, samym MCFA i MFCA z peptydem lizozymowym. Co więcej, MFCA + środek przeciwzapalny charakteryzował się największą różnorodnością mikroflory nosa i z kolei wykazywał najniższą częstość występowania choroby powodowanej przez S. suis. W przeprowadzonym przez nich badaniu na grupie loch, skład mikroflory zarówno w kale, jak i w przewodzie nosowym, zmienił się, co ponownie podkreśla znaczenie szerokiego podejścia: już od lochy aż do prosięcia.
To, czy dodatki paszowe mogą być dobrą alternatywą dla środków przeciwdrobnoustrojowych w obecnym scenariuszu dotyczącym S. suis, jest nadal kwestią otwartą, ale ostatnie dane uzasadniają dalsze badania nad tym zagadnieniem. Sformułowanie przekrojowych programów żywieniowych, które modulują mikroflorę i błoną śluzową przewodu pokarmowego w celu uzyskania prawidłowej równowagi, należy również włączyć do programu kontroli S. suis.



